重磅!广州永士达OCT导管获得两项广东创新医疗器械特别审批绿色通道
《创新医疗器械特别审批程序(试行)》政策背景?
为鼓励医疗器械的研究与创新,促进医疗器械新技术的推广和应用,推动医疗器械产业的发展,我国于2014年开始推行创新医疗器械特别审批程序(“特别审批程序”)。
医疗器械市场在国内起步较晚,但发展迅速,2001年至2014年,我国医疗器械市场规模从173亿元增长至2556亿元,增长了近15倍,复合增速达到23%。但从医疗器械市场规模与药品市场规模的对比来看,全球医疗器械市场规模大致为全球药品市场规模的40%,而我国这一比例低于15%,随着经济的发展以及国内老龄化程度的提高,医疗器械市场发展潜力巨大。同时,《创新医疗器械特别审批程序(试行)》等一批政策的出台,为国产创新医疗器械的快速成长奠定了坚实的基础。重点关注的细分领域包括:
1)与机器人、人工智能等先进技术相结合的高端医疗器械;
2)国产创新型医疗器械;
3)智能家用医疗器械;
4)现有成熟医疗器械的进口替代产品。

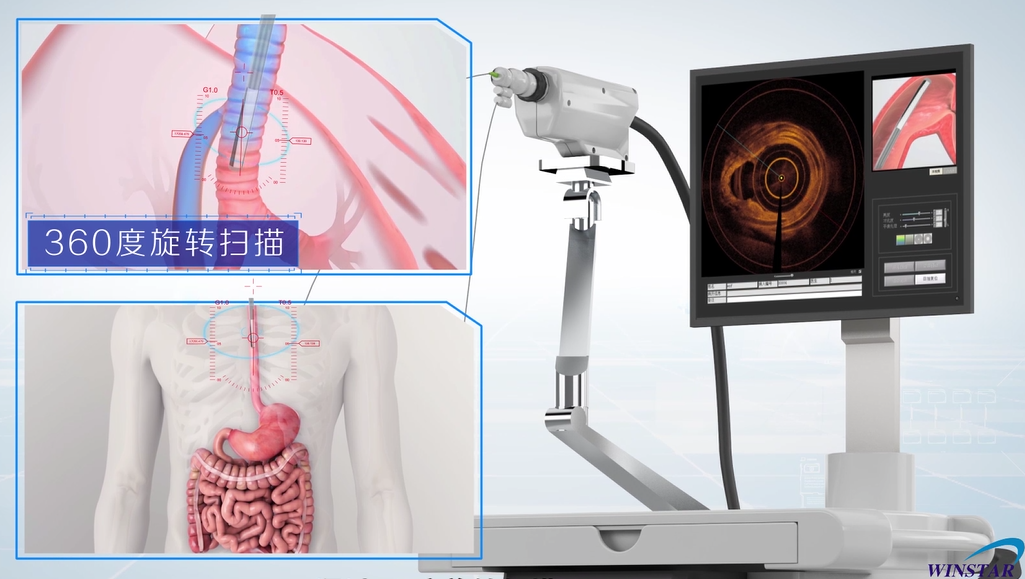
2016年11月,广州永士达医疗科技有限责任公司的OCT断层成像系统获得国家食品药品监督管理总局(CFDA)医疗器械技术审评中心批准进入《创新医疗器械特别审批程序》,成为我国首个获批进入特别审批绿色通道的OCT设备。2018年5月永士达OCT系统配套耗材“应用于呼吸道疾病检测的成像导管”和“应用于生殖道子宫内膜检测的成像导管“”又双双获得广东省局绿色通道批文。
获得《创新医疗器械特别审批程序(试行)》的好处?
CFDA将对永士达的相关申请予以优先办理,注册检验、注册质量体系核查、技术审查、行政审批流程时限分别缩减30%以上,这么高的效率,各位RA小伙伴是不是已经看得流口水了?当然这与企业后期的充分准备及审批过程中的高度配合密不可分!继续撸起袖子加油干吧!!



